黑色素瘤是源于黑色素细胞的一类恶性皮肤肿瘤,具有恶性程度极高、易复发、易转移等特性,是极难治愈的一类恶性癌症。近年来,癌症免疫疗法取得了巨大突破,其中肿瘤疫苗是极具临床前景的一类免疫疗法。但是,常规肿瘤疫苗受限于不同个体肿瘤抗原表达的巨大差异以及免疫响应不够强烈等,难以在临床进行推广。因此,如何针对癌症患者研制个性化肿瘤疫苗并增强机体的抗肿瘤免疫响应成为目前亟待解决的问题。近日,华中科技大学武汉光电国家研究中心张智红教授课题组和美国中央俄克拉荷马州立大学Wei R. Chen教授在生物医学1区杂志《Theranostics》(2018 IF: 8.063)上发表论文,报道一种激光免疫疗法 (Laser Immunotherapy, LIT),通过使用一种免疫刺激剂N-乙酰化壳聚糖 (N-dihydrogalactochitosan, 简称GC) ,并联合980 nm的近红外激光照射实现光热治疗 (Photothermal Therapy, PTT),可有效清除原位黑色素瘤,并抑制远端转移灶以及肿瘤的再次复发。利用活体动态光学成像技术和传统免疫学方法,对激光免疫治疗后机体的关键抗肿瘤免疫事件和形成长期抗肿瘤免疫记忆的相关机制进行深入研究。
在此项研究中,研究人员首先在瘤内注射免疫刺激剂GC,然后使用980 nm激光对肿瘤进行PTT治疗。瘤内GC迅速募集大量中性粒细胞到肿瘤区域,且大部分GC被中性粒细胞所摄取。黑色素瘤能够将980 nm激光的光能有效转换为热能,诱导肿瘤细胞的免疫原性死亡,释放大量损伤相关的分子伴侣 (Damage Associated Molecular Patterns, DAMPs), 提供全肿瘤细胞抗原。中性粒细胞在GC、DAMPs以及肿瘤抗原的作用下,与肿瘤区域的树突状细胞 (Dendritic Cell, DC) 相接触,促进DC对肿瘤抗原的摄取和成熟。成熟DC携带肿瘤抗原迁移到引流淋巴结中,进一步激活机体的系统性抗肿瘤免疫反应以及长期的肿瘤特异性免疫记忆。通过活体光学成像技术,对激光免疫治疗后40天的小鼠再次接种肿瘤的微环境进行动态监测,结果表明,机体的记忆性T细胞能够被迅速活化,转变成效应性T细胞,并大量效募集到肿瘤区域,运动非常活跃,从而实现对肿瘤细胞的识别和清除。
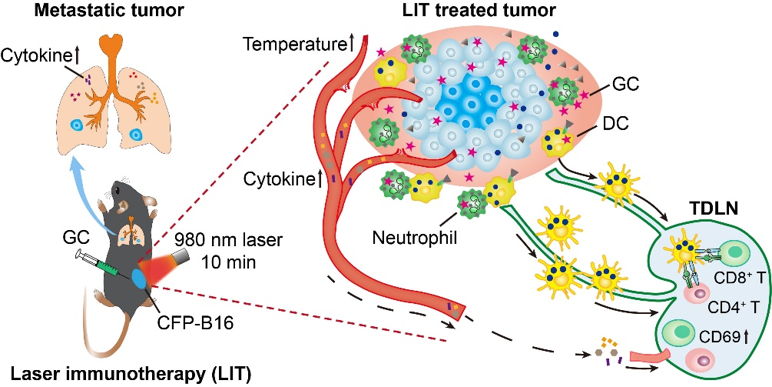
该研究利用激光免疫疗法实现对原位黑色素瘤的有效清除,诱导机体产生长期的肿瘤特异性免疫记忆,对再次皮下接种的肿瘤以及肺转移灶具有良好的抑制效果。将活体光学成像技术与免疫学方法相结合,对LIT如何诱导机体产生有效的抗肿瘤免疫应答以及建立长期肿瘤特异性免疫记忆的相关机制进行研究,为激光免疫疗法的临床应用和推广提供理论基础。
华中科技大学武汉光电国家研究中心张智红教授和美国中央俄克拉荷马州立大学Wei R. Chen教授为文章的共同通讯作者,课题组成员祁淑红博士后和卢利森博士为文章的并列第一作者。
参考文献:
Neutrophil infiltration and whole-cell vaccine elicited by N-dihydrogalactochitosan combined with NIR phototherapy to enhance antitumor immune response and T cell immune memory. Theranostics, 2020. 10(4):1814-1832.
原文链接:https://www.thno.org/v10p1814.htm