细胞的稳态离不开内部多种亚细胞结构的精确分工和协同合作,洞悉细胞内细胞器/蛋白分子的精密运转是一项重要的生命科学研究需求,为揭示发育、疾病等浩瀚生命现象的微观机制提供重要参考。借助荧光显微成像技术,人们得以实现对亚细胞结构的特异性观测,但因光学衍射极限的存在,成像的分辨率被限制在200纳米左右,这大大阻碍了对其精细结构的进一步探究。超分辨荧光显微成像技术的出现,使清晰观测亚细胞结构成为可能,但目前主流的超分辨荧光显微镜需通过多组图像测量来突破光学衍射极限,伴随着显著降低的时间分辨率和剧增的光毒性。对活细胞进行低侵入性、高时空分辨率的精细观测目前依然存在巨大的挑战。

针对上述问题,光电学院费鹏教授课题组联合武汉光电国家研究中心张玉慧教授课题组于2022年3月12日在Nature Methods在线发表题为Isotropic super-resolution light-sheet microscopy of dynamic intracellular structures at subsecond timescales的研究论文。文章提出了一种基于深度学习的超分辨荧光显微镜,实现对活细胞的精细动态和相互作用进行快速、三维、长时程地观测。
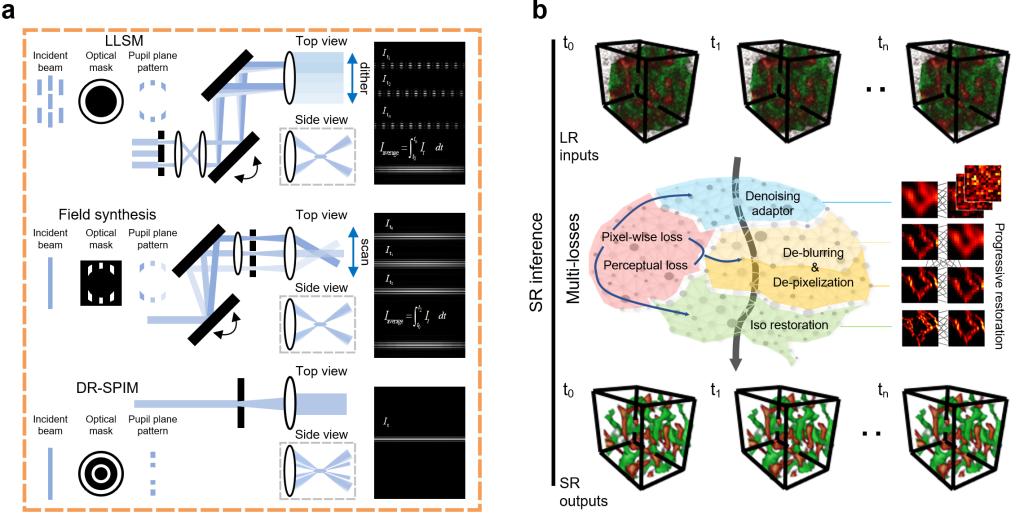
图1/ IDDR-SPIM成像技术的原理。a.经典Lattice光片、Field synthesis光片和本文双环光片产生原理和效果的对比;b.分而治之-协同优化的渐进式深度学习超分辨重建算法
研究在硬件上提出一种基于双环掩膜(Double-Ring, DR)调控的选择性光片照明方法(DR-SPIM),利用多级调制光的衍射显著抑制光片旁瓣的同时产生厚度仅为450纳米的超薄、静态、消色差光片,提供高轴向分辨率的原始三维图像并大幅度降低成像对活细胞的光毒性(图1a)。图像处理上,针对原始图像中噪声,衍射极限等多因素耦合造成的复杂降质,研究者们进一步提出各向同性、分而治之(Isotropic Divide-stage-to-process, ID)的计算重建新思路,构建了多段级联的卷积神经网络,先利用局部多级先验知识的分段训练精确模拟成像物理过程,再通过多种损失函数的联合优化对网络进行整体约束,将光学成像中固有的噪声、光学模糊、降采样、非均一性等降质问题联合求解,大幅度提升了算法在应对低信噪比-低分辨率图像时的增强性和精确性。最终基于单组带噪、衍射受限的光片图像即实时重建出高信噪比的超分辨图像。(图1b)。
光学和算法的软硬联合(IDDR-SPIM),克服了超分辨成像中时间和空间分辨率的相互妥协,无损速度地打破衍射极限,将活细胞三维成像空间分辨率提升到各向同性100纳米的同时实现视频速度的高时间分辨率。
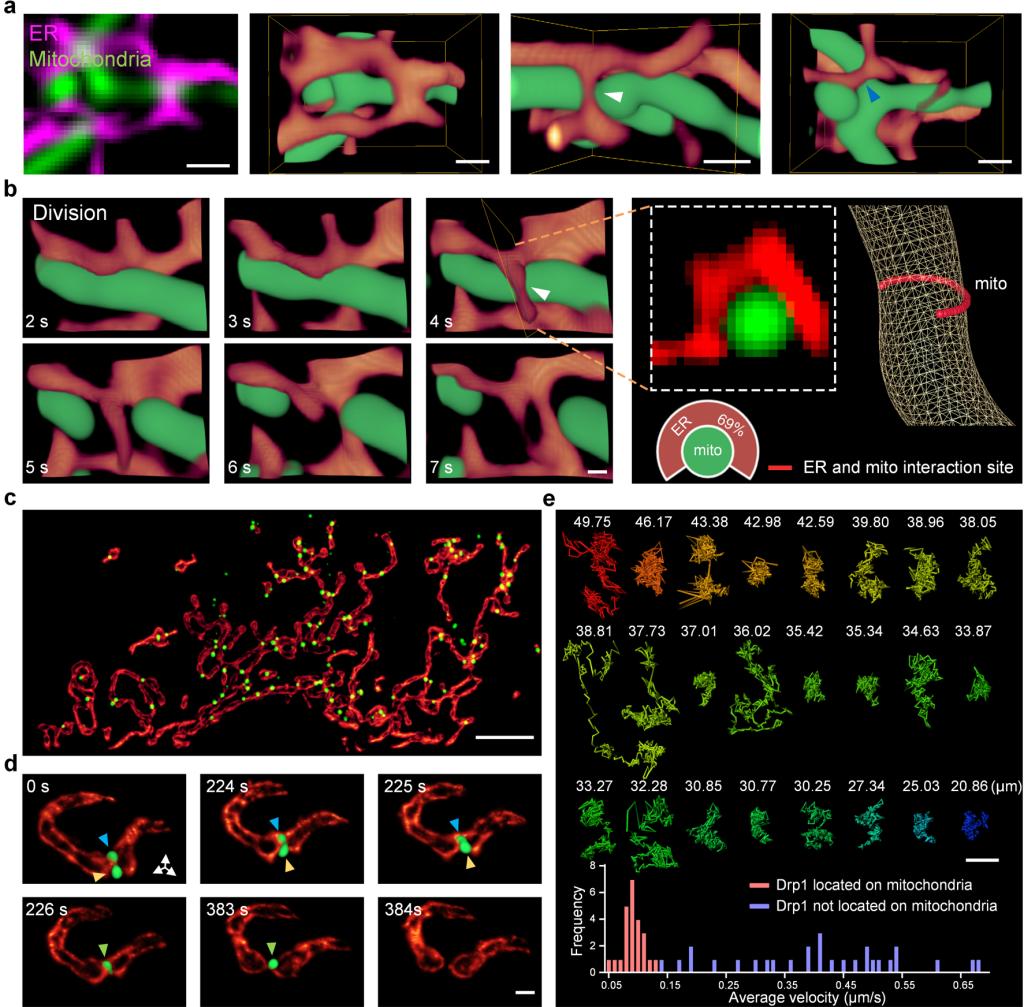
图2/ 五维(时间+三维空间+光谱)活细胞超分辨成像揭示线粒体/内质网,线粒体/Drp1寡聚体的三维动态相互作用。
研究人员进一步实现了GFP标记内质网和RFP标记线粒体结构的同步-三维-动态超分辨成像,捕捉到了内质网调控线粒体分裂的精细三维动态过程,并基于高时空分辨率的数据对内质网与线粒体的三维相互作用进行定量分析(图2a,b)。而得益于IDDR-SPIM成像极低的光漂白率,研究人员还对Drp1寡聚体调控线粒体分裂或分支的过程进行了持续观测,并分类表征了线粒体附着蛋白和游离蛋白在运动轨迹和速度上的不同(图2c-e)。由于蛋白寡聚体较细胞器结构体积更小,包含荧光分子更少,且在三维空间均存在运动,使用传统的超分辨显微镜均难以捕捉,更难以完成长时间观察。
简言之,该研究提出了一种新的光片超分辨显微成像策略,通过多级衍射调控的光片照明成像技术联合分而治之的深度学习单图超分辨算法,大幅突破现有三维超分辨成像的时空分辨率极限,为快速、三维、长时程地观测活细胞的精细动态和相互作用提供了强有力的新工具。
费鹏教授和张玉慧教授为本文共同通讯作者。费鹏课题组博士生赵宇轩、周瑶,张玉慧教授课题组博士后张朦、博士生张文婷为论文共同第一作者。本研究在基金委重大研究计划培育项目、基金委面上项目、国家重点研发计划、基金委重大仪器研制项目、武汉光电国家研究中心WNLO创新基金的资助下开展和完成。
论文链接:https://www.nature.com/articles/s41592-022-01395-5